La FDA, a través del Dr. Peter Marks, dijo en una entrevista difundida por abc News que la aprobación es cuestión de semanas y reveló que, según los ensayos clínicos, la respuesta inmune en niños de 12 a 15 años fue mejor que la observada en menores de 16 años en adelante; por lo cual están muy esperanzados de que la vacuna para niños de 5 a 12 también funcione muy bien.
No obstante, Marks dijo que su consejo más fuerte para los padres es que no busquen suministrar a los niños vacunas para adultos y pidió tiempo para que la FDA pueda hacer una mejor evaluación sobre la dosis correcta y segura para sus hijos.
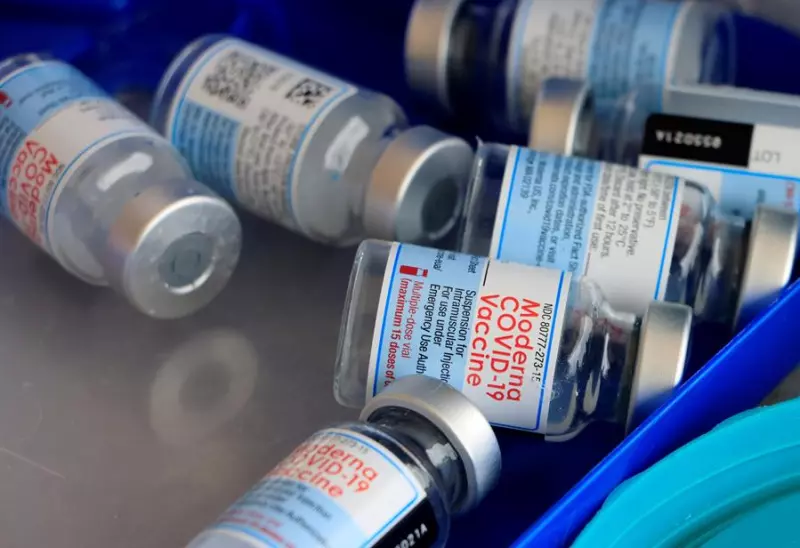
Medidas de la FDA sobre las vacunas COVID para niños
El representante de la FDA añadió que, si los padres quieren hacer algo para sus hijos, deben asegurarse de que todos los adultos y mayores de 16 años en el hogar estén vacunados y que sus niños sepan cómo usar correctamente los cubrebocas.
Actualmente, se siguen recopilando datos sobre las implicaciones de administrar el mismo tipo de antígeno que se usa para adultos, en menores de 12 años, aunque en menores dosis. La FDA, a principios de agosto, pidió seis meses de datos de seguridad de seguimiento, en lugar de los dos meses solicitados para los adultos.
Lo anterior se explica porque, en el caso de los ensayos para adultos, hubo más de 30,000 participantes, un número muy grande que permitió extrapolar los datos para hacer conclusiones significativas acerca de la seguridad de las vacunas.
De cualquier modo, Scott Gottlieb, excomisionado de la FDA y ahora parte de la junta directiva de Pfizer, dijo el domingo que habrá más datos relevantes sobre la eficacia de la vacuna en menores de entre 5 y 11 años, a finales de septiembre y que esperan que la FDA revise estos resultados en octubre.
La idea es que las vacunas para esta población se comiencen a aplicar a finales del otoño.
#QuéPasóCon las vacunas para menores